La edición genética sigue avanzando y dando alegrías a la
comunidad científica.
Un equipo dirigido por el español Juan Carlos Izpisúa,
del Laboratorio de Expresión Génica del Instituto Salk de EEUU, ha logrado por
primera vez introducir ADN en una localización concreta del genoma de células
que no se dividen, consiguiendo restaurar parcialmente la vista a roedores
ciegos.
El paso es importante no sólo porque es un avance importante para curar
la ceguera hereditaria, sino porque abre nuevas vías para la investigación
básica y para el tratamiento de enfermedades que afectan a otros órganos, como
cerebro, corazón o riñón.
En el estudio, que publica Nature, han participado
investigadores de varios países. Entre los españoles destaca la Universidad
Católica San Antonio de Murcia (UCAM), el Hospital Clinic de Barcelona y la
Clínica Cemtro de Madrid.Para entender la técnica que han desarrollado y su
importancia, hay que entender cómo funcionan las células. Hay varias
diferencias entre células que se dividen y las que no se dividen.
Cada una
tiene sus propios mecanismos para corregir el ADN.
Cuando una célula está en
división (como las de la piel o el intestino), usa un mecanismo denominado
recombinación homóloga (HDR, en inglés, reparación dirigida de homología), en
el cual el ADN puede ser sintetizado por un conjunto específico de proteínas.
Pero en el caso en el que las células detienen su proliferación (no se dividen,
como en el caso del corazón, el sistema nervioso o la retina) entra en acción
un mecanismo diferente en el ADN llamado unión de extremos no homólogos (NHEJ,
en inglés) y el sistema sólo liga los extremos rotos del ADN.Hasta ahora para
editar genes sólo se había utilizado el sistema de recombinación homóloga, por
lo tanto, en células que se dividen.
Los investigadores se centraron en esa vía
NHEJ y trabajaron para optimizar su maquinaria para usarla con el sistema
CRISPR-Cas9, el famoso corta-pega genético, que permite al ADN ser insertado en
localizaciones muy precisas dentro del genoma.
El equipo de Izpisúa creó un
paquete genético de inserción personalizado compuesto por un cóctel de ácidos
nucleicos que bautizaron como HITI (Homology-Independent Targeted Integration)
y usaron un virus inerte para insertarle el paquete de instrucciones genéticas
HITI a las neuronas de ratones adultos para comprobar que la técnica funcionaba
en células que no se dividen."Para que esta estrategia funcionara en un
lugar preciso del genoma, utilizamos el sistema CRISPR-Cas9, con lo que
generamos una ruptura en un sitio específico.
Luego al imitar los extremos
rotos del ADN interno en un ADN externo, el mecanismo de reparación normal de
la célula entra en acción y tenemos una célula que ya no se divide, pero
modificada con ADN nuevo de manera precisa. El simple hecho de usar el sistema
natural de las células que ya no se dividen (NHEJ) para hacer la corrección
dirigida es el mensaje principal de nuestras observaciones, ademas de hacer la
correción directamente in vivo en el organismo", explica Izpisúa a EL
MUNDO.
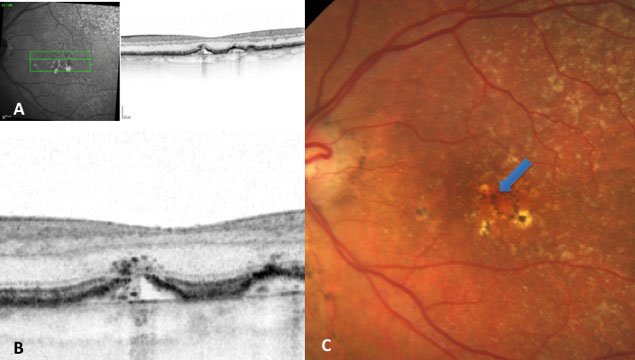
Para comprobar que servía también para la terapia de reemplazo de genes,
se aplicó en un modelo de rata para la retinosis pigmentaria, una condición
heredada de degeneración de la retina que puede causar ceguera en el ser
humano. Se insertó HITI en los ojos de ratas de tres semanas una copia correcta
de MERKT, uno de los genes que están dañados en la retinosis pigmentaria.
Cuando las ratas tenían ocho semanas los análisis mostraron que los animales
eran capaces de responder a la luz y superar varios tests que indicaban la
curación en las células de su retina.
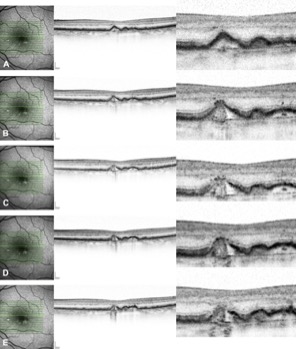
De izquierda a derecha, "mutante" (ojo ciego);
"corregido" (ojo reparado) y control" (ojo sano). UCAM
¿Por qué empezar por la retina?
Izpisúa indica que el ojo
es un órgano ideal para la terapia de reemplazo genético por su accesibilidad,
privilegios inmunológicos, pequeño tamaño o compartimentación. "Nosotros
podemos ver la retina a través de la pupila, puedes ver directamente la
enfermedad.
La prueba de concepto es mucho más fácil con una enfermedad que
puedes visualizar", explica Jerónimo Lajara, oftalmólogo y decano de la
Facultad de Ciencias de la Salud de la Universidad Católica San Antonio de
Murcia.Limitaciones e inconvenientes
En cuanto a las limitaciones del estudio,
Izpisúa señala que el principal inconveniente de HITI "es su eficacia en
vivo, que varía entre los tejidos diana (3%-20%).
Aunque las eficiencias son
mucho más altas que el enfoque basado en HDR existente, pueden no ser
suficientes para combatir enfermedades hereditarias donde las mutaciones
genéticas están afectando a una variedad de tejidos y órganos.
Además, para que
HITI trabaje más eficientemente en vivo, se necesita desarrollar en el futuro
un mejor sistema de inserción de genes".
En ese mismo sentido se manifiesta
Felipe Prósper Cardoso, director del Área de Terapia Celular y codirector de
Hematología de la Clínica Universidad de Navarra, al valorar el estudio.
"Conseguir la integración del gen y su expresión tiene todavía una
eficiencia limitada.
El gen que se introduce y va a corregir es como si fuera
una bala, por decirlo así, pero debe ir en una pistola que es el vector
adenoviral o adenovirus y éste tiene sus limitaciones.
Es necesario optimizarlo
viendo que se introduce en las células que queremos corregir y sólo en esas
células y en un número suficiente.
En cualquier caso, el trabajo abre nuevas
expectativas de edición génica in vivo".
El doctor Prósper añade que, tal y
como se indica en el trabajo, "la técnica corrige el gen, pero no cura la
enfermedad.
Se pueden corregir los genes pero si está muy avanzada la
enfermedad y hay muchas células que no son recuperables, la terapia puede no
ser eficaz. Por eso hay que corregirlos en estadios tempranos".
Por el
momento se van a obtener los permisos para la investigación clínica -en
personas-, proceso que podría llevar un año según Lajara. Después se aplicará a
otras enfermedades, "sobre todo en las que se originan por una
modificación en genes que se asocian inequívocamente a una enfermedad",
indica Izpisúa.
En la actualidad existen más de 5.000 enfermedades de este tipo,
la mayoría con baja prevalencia y por ello denominadas enfermedades raras, para
las que no hay un tratamiento curativo. "Ahora tenemos una tecnología que
nos permite modificar el ADN de las células que no se dividen para arreglar
genes en el cerebro, corazón e hígado", asegura Izpisúa, y añade:
"Nos permite por primera vez ser capaces de soñar con curar enfermedades
que antes no podíamos, lo cual es emocionante".